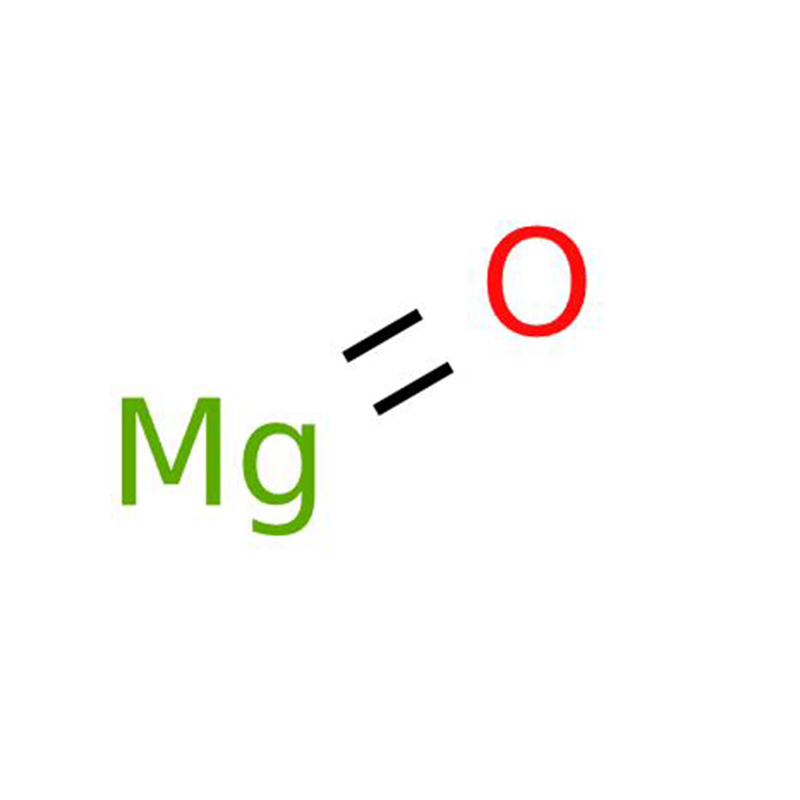
Magnesiumoxid CAS-Nr. 1309-48-4
Außergewöhnliche thermische Stabilität– Ultrahoher Schmelzpunkt (2.852 °C) für feuerfeste Auskleidungen und Tiegel.
Vielseitiger Industriezusatz– Verbessert die Gummi-/Kunststoffeigenschaften und wirkt als Katalysator oder Siliziumstahl-Separator.
Flammhemmende Eigenschaften– Wird in Baumaterialien verwendet, um die Feuerbeständigkeit zu verbessern.
Medizinische und landwirtschaftliche Leistungen– Wirksames Antazidum und Magnesiumergänzung für Boden und Futter.
Maßgeschneiderte Werkstoffqualitäten– Leichte (große Oberfläche) und schwere (hohe Dichte) Formen für spezielle Anwendungen.
Magnesiumoxid, oft auch Magnesia oder einfach Magnesiumoxid genannt, ist ein klassisches Erdalkalimetalloxid mit der chemischen Formel MgO. Diese weiße Pulversubstanz hat einen Schmelzpunkt von 2852 °C, einen Siedepunkt von 3600 °C und eine relative Dichte von 3,58 (25 °C). Es ist in sauren Lösungen und Ammoniumsalzlösungen löslich und reagiert allmählich mit Wasser zu Magnesiumhydroxid. In einer wässrigen Kohlendioxidlösung bildet es Magnesiumbicarbonat. Die Verbindung absorbiert mit der Zeit Feuchtigkeit und Kohlendioxid aus der Atmosphäre und setzt beim Erhitzen reizende Dämpfe frei.
Die Hauptquellen für die Magnesiumoxidproduktion sind Magnesit (MgCO₃), Dolomit (MgCO₃·CaCO₃) und Meerwasser. Der Herstellungsprozess umfasst die thermische Zersetzung von Magnesit oder Dolomit. Alternativ liefert mit Calciumhydroxid behandeltes Meerwasser Magnesiumhydroxidniederschlag, der anschließend kalziniert wird, um Magnesiumoxid zu gewinnen. Ein weiteres Produktionsverfahren nutzt Magnesiumchloridsole, die nach Bromextraktion aus Meerwasser oder Sole gewonnen wird. Durch Zugabe von Natriumhydroxid oder Natriumcarbonat entsteht Magnesiumhydroxid oder basischer Magnesiumcarbonatniederschlag, der anschließend zu Magnesiumoxid verbrannt wird. Derzeit verwendet China hauptsächlich Magnesit, Dolomit, Sole oder Soleblöcke als Rohstoffe.
Magnesiumoxid wird von allen Magnesiumverbindungen am häufigsten produziert und macht etwa drei Viertel aller industriellen Magnesiumprodukte aus. Magnesiumoxid, das unter 900 °C hergestellt wird, gilt als leichtes Magnesiumoxid und zeichnet sich durch geringe Dichte, große spezifische Oberfläche und hohe Adsorptionskapazität aus. In dieser Form dient es vielfältigen Zwecken: als Katalysator, als Gummizusatz zur Verbesserung der Eigenschaften und als Bestandteil von Magnesiumzement, wenn es mit Magnesiumchloridlösung gemischt wird. Es dient als Flammschutzmittel in Baumaterialien, als Antazidum und Abführmittel in der Medizin (insbesondere bei Übersäuerung und Magen-/Zwölffingerdarmgeschwüren, oft in Kombination mit stopfendem Calciumcarbonat) sowie als Zusatz in Tierfutter und Pflanzendüngern.
Leichtes Magnesiumoxid, das zwischen 950 und 1050 °C hergestellt wird, weist eine höhere Dichte und eine spezifische Partikelgrößenverteilung auf und ist dadurch besser wasserverträglich. Diese Variante dient als Trennmittel für Siliziumstahlplatten und verhindert das Sintern bei der Hochtemperaturverarbeitung, indem sie mit oberflächlichem Siliziumdioxid reagiert und eine Magnesiumsilikatschicht bildet. Schweres Magnesiumoxid, das bei 1500 bis 1800 °C hergestellt wird, zeichnet sich durch eine hohe Dichte, minimale spezifische Oberfläche, außergewöhnliche thermische Stabilität und reduzierte chemische Reaktivität (mit geringerer Säurereaktivität und Hydratationsrate) aus und eignet sich daher für feuerfeste Hochtemperaturanwendungen, einschließlich der Herstellung von feuerfesten Tiegeln und Ofenauskleidungen.